生活污水臭氧深度处理试验
摘要:
以生活污水处理厂二级生物处理出水为研究对象,利用固相萃取、吸附树脂层析等手段,研究了臭氧氧化过程中进出水及不同分级组分的发光细菌急性毒性的变化,揭示了无机离子浓度对臭氧氧化出水急性毒性的影响,并采用三维荧光光谱对急性毒性相关的物质组分进行了解析。结果表明,在反应时间为15 min,臭氧投加速率为2.1 mg·(L·min)-1,臭氧氧化出水的急性毒性明显下降,出水的急性毒性仅为进水的24.7%。水样不同分级组分的生物毒性测试结果显示,生物处理出水中的亲水性物质和疏水中性物质分别贡献了44.6%和27.8%的毒性当量。当生物处理出水的氯离子含量为75~400 mg·L-1时,经臭氧氧化后,出水的急性生物毒性与氯离子浓度成正相关关系,当生物处理出水的硫酸根离子和硝酸根离子含量分别在150~300 mg·L-1和20~110 mg·L-1变化时,经臭氧氧化后,出水的急性生物毒性变化不大,结合三维荧光光谱的分析结果,臭氧氧化出水中急性毒性物质可能主要存在于芳香族蛋白质类似物(Ⅱ区)和类腐殖酸类物质(Ⅴ区)中。
正文:
我国是世界上水资源短缺很为严重的国家之一,城市污水回用是解决水资源短缺的有效途径[1]。城镇生活污水的处理以生物法为主,出水水质通常不能满足回用水的要求,需要深度处理,以进一步去除水中微量有机污染物、悬浮物、氮和磷等。臭氧深度处理是一种简单、有效的深度处理技术,反应快且无二次污染,常用于生活污水的深度处理。针对如何评价和表征处理后回用水的水质安全风险问题[2-4],研究者主要采用生物毒性作为物理化学指标的补充。急性生物毒性是指人、鱼类、细菌和藻类等生物体在一次或在24h内多次与毒性物质接触后,短期内产生的致毒效应。水体中含有各种无机离子和有机物,水体中的氯离子、硫酸根离子和硝酸根离子,有可能与高级氧化过程中产生的·OH等发生反应,MUTH-UKUMAR等在处理染料废水中报道[5],臭氧氧化中的臭氧、·OH和水体中的无机离子会发生反应。但是目前针对生活污水的臭氧深度处理研究中,缺乏对臭氧深度处理对出水急性毒性的影响因素的研究。
本实验采用臭氧氧化深度处理生活污水,研究臭氧氧化对生活污水的急性毒性变化的影响,考察水中无机离子对臭氧氧化深度处理生活污水急性毒性的影响,并对产生毒性的主要物质组分进行了分离,以识别关键的生物毒性组分。
1 材料与方法
1.1 实验装置
本研究的实验装置如图1所示。臭氧发生器产生臭氧,臭氧接触柱由玻璃制作,总高1.3m,内部直径3.56cm。接触柱内部中空,底部设有气室,采用多孔钛板均匀曝气。接触柱采用下层进气、上层进水,水气交错,以增大接触面积和接触时间。臭氧反应的温度在室温25℃,反应时间为15min,臭氧投加速率为2.1mg·L-1·min-1。
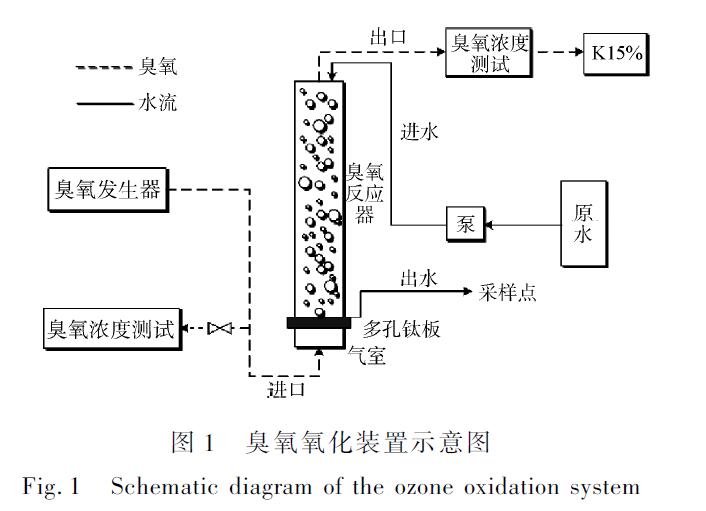
1.2实验用水
实验用水为某校园生活污水二级生物处理出水,其水质情况如表1所示。
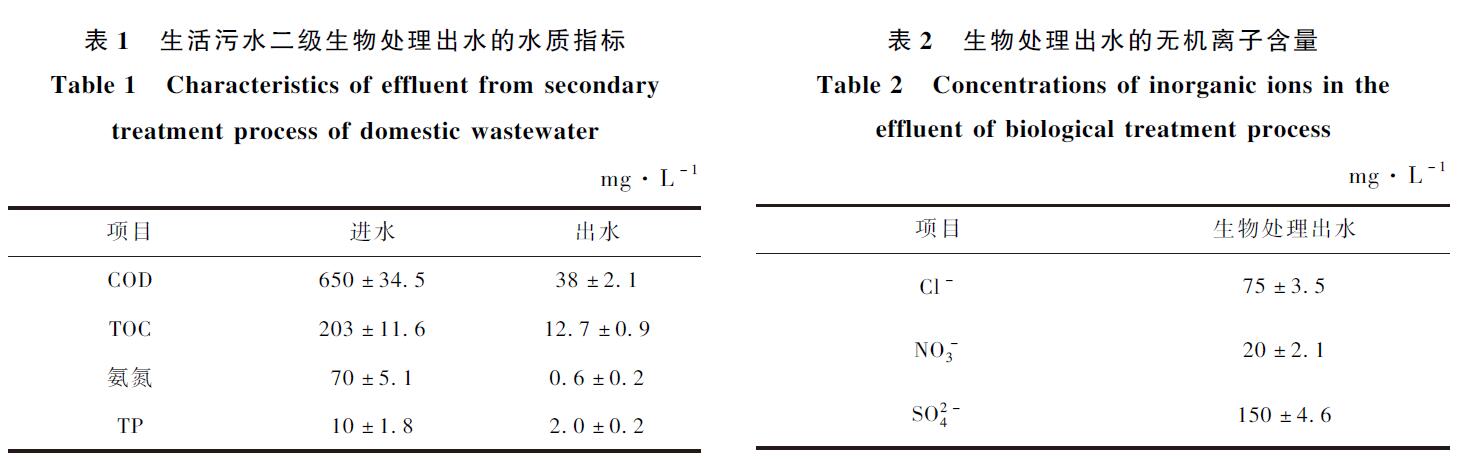
生物处理出水中的3种无机离子的浓度如表2所示。
为考察水中无机离子对臭氧氧化处理生活污水急性毒性的影响,在上述出水水样中人工投加了一定量的氯离子、硫酸根离子和硝酸根离子,配置以下模拟水样,如表3所示。

1.3 水质指标的测定
水样的COD、TOC、氨氮和总磷的测定方法采用国家标准方法[6]:COD采用微回流消解比色法测定(Hach DR890,USA);TOC采用岛津TOC分析仪测定(Shimadzu TOC-VCPH,Japan);氨氮采用水杨酸-次氯酸盐分光光度法测定;总磷采用过硫酸钾消解-钼锐抗分光光度法测定;气相中臭氧浓度的测定方法参考《臭氧发生器臭氧浓度、产量、电耗的测量CJ/T3028.2-1994》,液相中的臭氧浓度采用靛蓝法检测。
1.4 急性毒性测试
急性毒性测试选用青海弧菌Q67(Vibrioqinghaiensis sp.Q67)[7-9]为指示生物。发光细菌毒性检测是一种操作简单、反应快速和灵敏度高的方法,已被广泛应用于环境污染物急性毒性的研究[10]。
首先调节各水样pH值范围为7.0~8.0,然后进行固相萃取,选用6mL,500mg的HLB固相萃取小柱(Waters Oasis,USA)分别用正己烷、二氯甲烷、甲醇洗脱得到总洗脱混合液,将混合液旋转蒸发浓缩至1~2mL,氮气吹干后,分别用200uL二甲基亚矾(DMSO)复溶。实验前配置毒性实验测试方法中需要的稀释水,稀释水配方为:CaCl2,11.1mg,KCl4.2mg,NaHCO3,42mg,MgSO4,28.6mg,NaNO34.1ug溶于1L超纯水中。然后用稀释水稀释待测样品,设10个稀释度,每个稀释度做3个平行,以模拟湖水为空白对照,将待测样品和菌悬液混匀15min后用酶标仪(Tecan infinite-200)测定相对发光度RLU(relative lightunits),计算样品的相对发光抑制率:
相对抑制率(%)=(1-试样的RLU/空白对照的RLU)×100
以样品的相对发光抑制率对样品的稀释倍数作图,求出样品的EC50值,即很大毒性效应的半数效应浓度,急性毒性单位定义为:1TU=EC50-1
1.5吸附树脂分离
参考文献中的方法[7],将水样经0.45um的微孔滤膜过滤后,通过XAD-8吸附树脂层析柱(Φ=1.6cm,H=20cm,体积为40mL),流出液储存备用,用0.1mol·L-1HC1反冲洗树脂柱,得到疏水碱性组分(HOB)。再将流出液用浓盐酸调节pH至2.0±0.1,并再次通过树脂柱,流出的组分为亲水性组分(HIS),再用0.1mol·L-1NaOH反冲洗树脂柱,得到疏水酸性组分(HOA),很后用甲醇反复洗脱树脂柱,得到疏水中性组分(HON)。
1.6三维荧光光谱扫描
对水样进行三维荧光光谱(HitachiF4500型荧光光谱分析仪)扫描。扫描条件为激发光源:150-W氩弧灯;PMT电压:750V;扫描间隔:Ex=5nm,Em=10nm;采用自动响应时间,扫描速度为30000nm·min-1,激发和发射波长范围:Ex=200~400nm,Em=280~550nm,以超纯水做空白对照。用Origin8.5软件对扫描得到的每个发射/激发波长下的荧光强度数据进行处理,将得到的三维数据矩阵作等值线图,EEM的积分方法参考CHEN[11]的荧光区域积分方法(FRI)。
点击下载:生活污水的臭氧深度处理及其急性毒性PDF
参考文献(共18条):
[1] 陈亚萍, 康永祥. 城市污水回用及其途径[J]. 干旱区研究, 2005, 22(3):382-386
[2] 余若祯, 穆玉峰, 王海燕, 等. 排水综合评价中的生物毒性测试技术[J]. 环境科学研究, 2014, 27(4):390-397
[3] 胡洪营, 吴乾元, 杨扬, 等. 面向毒性控制的工业废水水质安全评价与管理方法[J]. 环境工程技术学报, 2011, 1(1):46-51
[4] LIBRALATO G, ANNAMARIA V G, Francesco A. How toxic is toxic? A proposal for wastewater toxicity hazard assessment[J]. Ecotoxicology & Environmental Safety, 2010, 73(7):1602-1611
[5] MUTHUKUMAR M, SELVAKUMAR N. Studies on the effect of inorganic salts on decolouration of acid dye effluents by ozonation[J]. Dyes & Pigments, 2004, 62(3):221-228
[6] 国家环境保护总局. 水和废水监测分析方法[M]. 第4版. 北京:中国环境科学出版社, 2002:211-281
[7] 孙迎雪, 吴乾元, 田杰, 等. 污水中溶解性有机物组分特性及其氯消毒副产物生成潜能[J]. 环境科学, 2009, 30(8):2282-2287
[8] 马梅, 童中华, 王子健, 等. 新型淡水发光菌(Vibrio qinghaiensis sp. Q67)应用于环境样品毒性测试的初步研究[J]. 环境科学学报, 1998, 18(1):88-93
[9] 朱文杰, 汪杰, 陈晓耘, 等. 发光细菌一新种——青海弧菌[J]. 海洋与湖沼, 1994, 25(3):273-279
[10] 卓平清, 王弋博, 薛林贵, 等. 青海弧菌在环境污染物监测中的应用研究进展[J]. 天水师范学院学报, 2014, 34(2):22-26
[11] CHEN W, WESTERHOFF P, LEENHEER J A, et al. Fluorescence excitation-emission matrix regional integration to quantify spectra for dissolved organic matter[J]. Environmental Science & Technology, 2003, 37(24):5701-5710
[12] BELTRÁN F J, GARCÍA-ARAYA J F, ÁLVAREZ P M. pH sequential ozonation of domestic and wine-distillery wastewaters[J]. Water Research, 2001, 35(4):929-936
[13] COBLE P G, GREEN S A, BLOUGH N V, et al. Characterization of dissolved organic matter in the Black Sea by fluorescence spectroscopy[J]. Nature, 1990, 348:432-435
[14] HER N, AMY G, MCKNIGHT D. Characterization of DOM as a function of MW by fluorescence EEM and HPLC-SEC using UVA, DOC, and fluorescence detection[J]. Water Research, 2003, 37(17):4295-4303
[15] WU F, EVANS R, DILLON P. Separation and characterization of NOM by high-performance liquid chromatography and on-line three-dimensional excitation emission matrix fluorescence detection[J]. Environmental Science & Technology, 2003, 37(16):3687-3693
[16] HUDSON N, BAKER A, REYNOLDS D. Fluorescence analysis of dissolved organic matter in natural, waste and polluted waters-A review[J]. River Research and Applications, 2007, 23(6):631-649
[17] HENDERSON R K, BAKER A, MURPHY K R, et al. Fluorescence as a potential monitoring tool for recycled water systems:A review[J]. Water Research, 2009, 43(4):863-881
[18] 孔赟, 朱亮, 吕梅乐, 等. 三维荧光光谱技术在水环境修复和废水处理中的应用[J]. 生态环境学报, 2012, 21(9):1647-1654
[19]张松,李菲菲,史晨,胡翔,朱小彪,生活污水的臭氧深度处理及其急性毒性,环境工程学报,1673-9108(2017)06-3468-7



 当前位置:
当前位置: 
 摘要
摘要


 上一篇:
上一篇: 返回列表
返回列表
